

Números cuánticos
¿Qué son los números cuánticos?
Los números cuánticos son valores numéricos que nos indican las características de los electrones de los átomos, basado en la teoría atómica de Neils Bohr.
Cada electrón del átomo está representado por cuatro números cuánticos:
n
l
ml
ms

número
cuántico
principal
número
cuántico
orbital
número
cuántico
mágnetico
número
cuántico
de spin

Número cuántico principal
(n) solo puede tomar valores naturales:
1, 2, 3, 4, 5, 6 y 7
Cada valor designa el nivel o periodo, el cual está relacionado con el tamaño y la energía del orbital.

¿Quieres saber qué es un orbital?
Da clic AQUÍ

Sus valores dependen del valor de l, de manera que:
s: 0
p: -1,0,+1
d: -2,-1,0,+1,+2
f: -3,-2,-1,0,+1+2,+3
Está relacionado con la orientación del orbital en el espacio

Número cuántico magnético
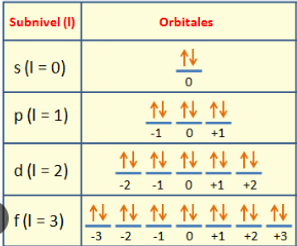

Número cuántico orbital
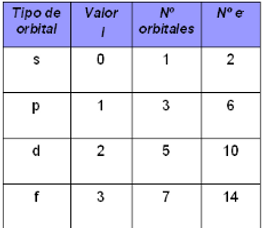
(l) toma valores enteros :
s = 0: con capacidad para 2 electrones
p = 1: con capacidad para 6 electrones
d = 2: con capacidad para 10 electrones
f = 3: con capacidad para 14 electrones
Este número está relacionado con la forma del orbital que ocupa el electrón.

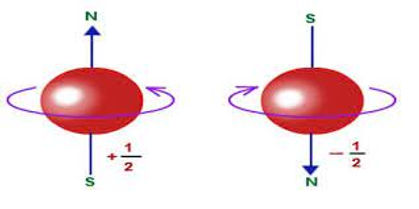
Número cuántico de spin

Solo puede tomar los valores:
+ 1/2
- 1/2
Está relacionado con el giro del electrón respecto a su eje.

Distribución electrónica

La configuración electrónica fundamental se obtiene, en la práctica, a partir de tres reglas o principios:

1. Regla de construcción
3. Regla de la máxima multiplicidad de Hund
2. Principio de exclusión de Pauli
"La configuración electrónica fundamental se determina colocando los electrones individualmente en los orbitales disponibles del átomo en secuencia ascendente de energía."
"Dos electrones de un mismo átomo no pueden tener los cuatro números cuánticos iguales."
"Cuando múltiples electrones ocupan orbitales degenerados de la misma energía, lo hacen en orbitales distintos y con spines paralelos, siempre que sea posible."

Diagrama de Moeller

¿Quieres aprender jugando?
Escanea el Qr


Prueba de la Unidad 1


